《Genet法說筆記》高端疫苗(6547) 腸病毒71型疫 2021年的獲利關鍵 投資人如何追蹤?
日期 : 2020/1/3
作者 : 夏彌新(生技醫療第一站)
基本資料
1. 2012年10月成立
2. 2018年04月上櫃
3. 股本為15.6億台幣
4. 主要為疫苗和生物製劑的開發和商業化
公司核心技術:
現在公司細胞培養疫苗量產廠是台灣的第一座
高端疫苗主要的核心技術聚焦在「細胞培養」的製程優化與後續量產,新型的細胞培養技術是採用選定的細胞株代替傳統動物活體組織,作為病毒感染媒介並藉以量產疫苗。
腸病毒71型疫
1. 東南亞市場: 腸病毒71型病毒容易引發神經系統的併發症,而六個月以下嬰兒具最高的重症、死亡率,重症致死率達三程。高端瞄準腸病毒盛行的馬、星、越、泰和菲五國的東南亞市場,當地目標市場的新生兒人口就有535萬人。(簡報圖)
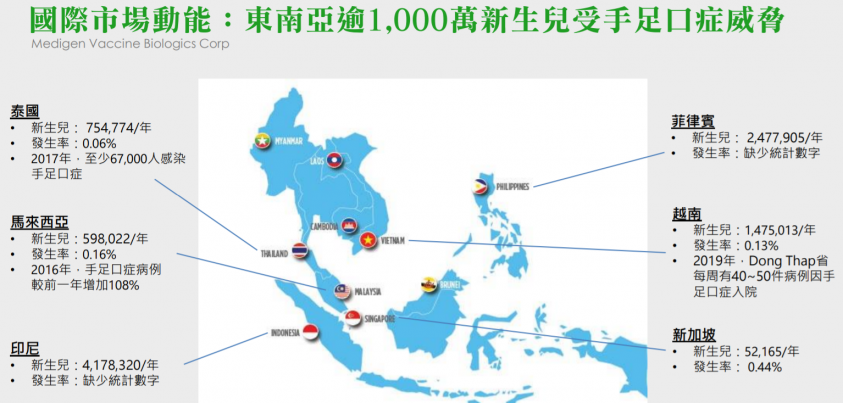
2. 高端的競爭優勢
臨床試驗設計,包括東協多國多中心大型臨床試驗、臨床設計將驗證是否可用於2-6個月嬰幼兒疫苗等,臨床試驗三期試驗進行中,預計12月完成收案。二期臨床試驗數據佳,待三期臨床試驗大族群的驗證。

3. 臨床試驗設計
有兩個指標,主要指標的臨床療效 (EV71疾病事件)以及次要指標:免疫生成性、交叉反應性、批次一致性、安全性,但是台灣現在有鼓勵政策,所以只要觀察接受施打後六個月血中抗原量是否達標,台灣就可先行申請藥證,至於東南亞藥證需要看六個月發病是否達標。

4. 藥證申請
預計今年底, 超過3000受試者的完整臨床療效指標必須觀察六個月後的免疫生成性,即可在2020年的年中分析,並申請 rolling review。法人估,台灣:2021; 東南亞: 2021-2022。



.jpg)

