【讀者提問】高端疫苗(6547)新冠疫苗6/10日進行二期期中分析解盲 期中分析就可以取得TFDA緊急使用授權(EUA)?
最近大家都在期待高端疫苗新冠疫苗二期臨床試驗的結果,如果符合台灣TFDA的「期望」,將有機會取得台灣TFDA給予緊急使用授權EUA,之後台灣民眾就可以開始施打國產疫苗。
有讀者來函詢問,甚麼是疫苗保護力(efficacy)? 期中分析代表甚麼含意? 這樣二期算不算完成??
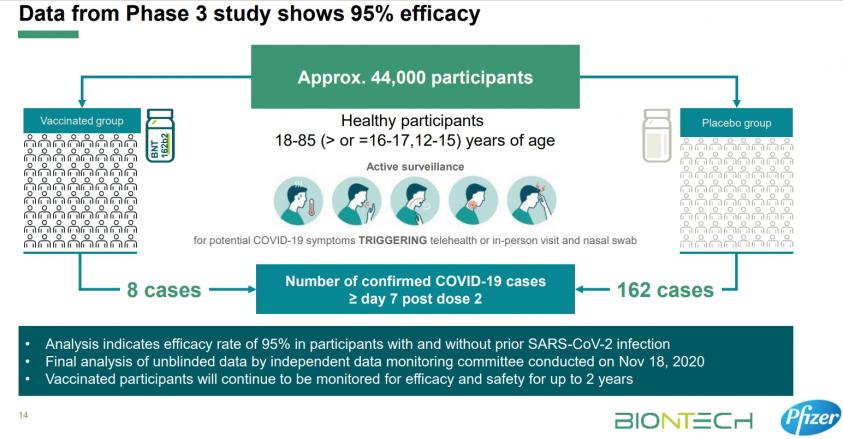
1. Efficacy 要在疫區試驗才有可能計算,四月底前,台灣還不是疫區。(下圖:輝瑞Efficacy保護力)
2. 高端的期中分析將提出安全性與免疫生成性評估數據給獨立專家委員會
期中分析有三種可能: 繼續進行試驗( Continue as plan)、建議修改臨床試驗(Modify protocol)-增加人數或延長研究時間,或是停止(Terminate )。停止試驗常見三個原因,有非常顯著的效果(Robust efficacious),或是繼續進行試驗也是徒勞無功(Futility),也有可能是發現藥物安全性的問題(Dangerous),上述原因都可能讓試驗提早結束。
3. 高端疫苗能否一二期臨床試驗的期中分析取得TFDA的緊急使用授權EUA,這要看台灣TFDA的態度。
4. 高端疫苗是能防止感染還是預防重症?
Efficay:參考輝瑞/BNT三期臨床試驗期中分數據示意圖-約四萬四千受試者在疫區執行,FDA看的不是中和抗體的產生,而是看到疫苗可以有效預防新冠的發生,以下是在總體人群中觀察到的疫苗效力。
|
說明及澄清媒體報導: 110/06/08 12:46:40 事實發生日:110/06/08
2.公司名稱:高端疫苗生物製劑股份有限公司
3.與公司關係(請輸入本公司或子公司):本公司
4.相互持股比例:不適用
5.傳播媒體名稱:聯合報第A01版
6.報導內容:
高端疫苗也預計最快六月十日解盲。……熟悉生技醫療產業的基金經理人表示,二期臨床解盲只會公布疫苗安全性和中和抗體濃度,不會有外界關切的疫苗保護力(Efficacy)比率。……高端指出,進行試驗的醫學中心和實驗室已在五月底完成第二劑施打及一個月觀察期,現正等待國外臨床試驗公司彙整安全性及免疫生成性等資料,提交到藥廠的獨立專家委員會解盲,預計六月十日、最晚不超過六月十五日。
7.發生緣由:
本公司新冠肺炎疫苗二期臨床主試驗,在4/28完成所有受試者第二劑疫苗施打後,按藥證主管機關之技術性要求及臨床試驗設計,已於5/28達到「所有受試者第二劑疫苗施打後一個月、以及中位數受試者追蹤二個月」之期間/期中分析(Interim Analysis)條件。
期間/ 期中分析之安全性與免疫生成性評估數據,本公司與臨床試驗中心皆在盲性狀態下,交由第三方單位(CRO,臨床試驗受託機構)進行資料清理,預期近期內完成資料彙整,並召開IDMC獨立資料監視委員會,以進行期間/期中分析解盲作業,後續研發進度本公司將依規定進行公告。
|





