《Genet法說筆記》北極星(6550)回應提問:ADI-PEG20肺間皮癌美國取證後銷售規劃?日本與中國臨床試驗將鎖定何種適應症?
北極星(6550)於3/9舉辦線上法人說明會,會中陳鴻文董事長針對旗下ADI-PEG20各項臨床試驗進展以及公司未來在新藥與CDMO的發展策略上進行說明,Genet為大家整理相關重點。
延伸閱讀:《Genet法說筆記》北極星(6550)代謝療法ADI-PEG20肺間皮癌3月底pre-BLA會議拼今年取證!軟組織肉瘤臨床三期啟動收案!
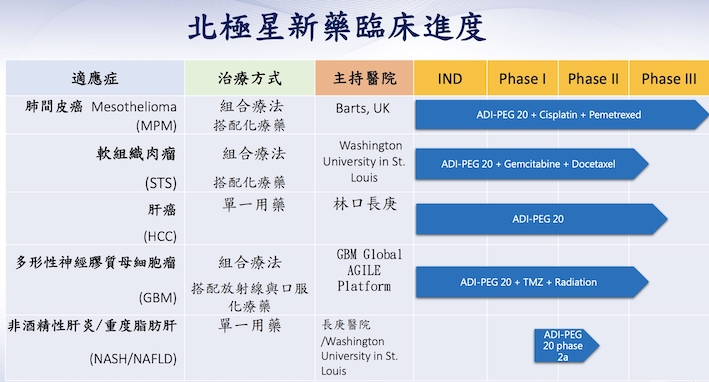
關於北極星藥業(6550):北極星核心產品為癌症新藥ADI-PEG20,主要是針對精氨酸(L-Arginine)抑制劑機轉所設計出的標靶型抗癌藥物,目前以惡質肺間皮癌、軟組織肉瘤、肝癌、腦癌等癌症為主要適應症,各適應症的人體臨床實驗均在進行中。
針對本次會後投資人對於北極星營運上的提問以及公司回覆,整理如下:
問一:公司是否有信心肺間皮癌的解盲數據可被FDA認可並成功取證?
問二:肺間皮癌美國成功取證後的市場銷售規劃?
問三:軟組織肉瘤臨床三期試驗原訂二月收案,目前延遲的原因?
問四:腦癌臨床二期試驗目前台灣與韓國預計何時收案?
問五:日本與中國將開展的臨床試驗是鎖定哪些適應症?
問六:非酒精性肝炎(NASH)臨床IIA試驗預計用藥多久可見療效?
問七:宜蘭新廠預計何時可以動工?
問八:公司2023年營業費用預估?主要會用在哪些適應症?
問一:公司是否有信心肺間皮癌的解盲數據可被FDA認可並成功取證?...


.jpg)
.jpg)
