《生物相似藥》市場競爭越趨白熱化!美國已核准生物相似藥達35個 (表)!
日期 : 2022/3/8
作者 : 蔡雪綸(生技投資第一站)
生物相似藥在美國稱為Biosimilars或是Follow-on biologics,意即當原廠的生物製劑(大分子蛋白質藥物)專利到期後,其他生物製藥公司可以參考其分子結構特性來研發生產具有相似臨床療效的藥物。(Genet專欄: 科技廠跨足bio-CDMO 三星生物磨10年,從門外漢變一哥)
生物相似藥的基本法律框架為2009年生物製品價格競爭與創新法案(BPCI Act),該法案於2010年3月23日由美國時任奧巴馬總統簽署成為正式法律,致力為那些與美國FDA已核准之生物製劑『高度相似』或『可互換』的生物產品建立一個簡易的批准途徑。
延伸閱讀:《生物相似藥》大戰原廠藥!雙方營銷策略與廣告支出你消我長?醫師與病患:療效與安全性才是關鍵!
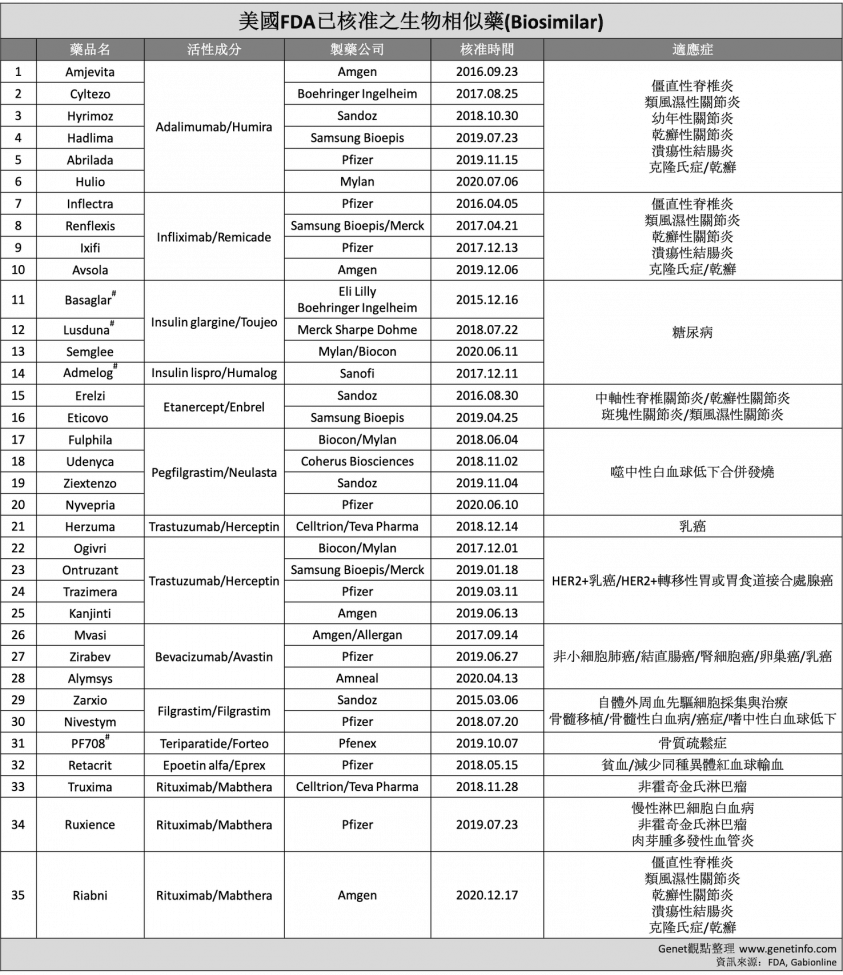
山德士(Sandoz)所開發的Zarxio (filgrastim-sndz)於2015年成為美國第一個獲准的生物相似藥產品,迄今為止,FDA已批准的生物相似藥包含以下產品類別:(1)抗腫瘤壞死因子-α(TNF-α);(2)單株抗體(mAbs);(3)白血球生長激素(G-CSF)以及(4)胰島素的後續生物製品(Admelog、Basaglar、Lusduna 和 Semglee)與特立帕肽(PF708)。下表為當前美國已核准上市之35個生物相似藥清單:
延伸閱讀:《生物相似藥》全球霸主! Sandoz 全球營運總監Pierre Bourdage宣示 2030年銷售將躍升三倍至60億美元
資料來源:FDA, Gabionline
更多資訊,請參考今日彙整。





