《FDA》癌症風險浮現! 藍鳥生物 (Bluebird bio) 終止腎上腺腦白質退化症 (ALD) 基因療法臨床試驗
秒速閱讀: 基因療法雖然有效,但也面臨安全性與高價位的難題。
腎上腺腦白質退化症 (Adrenoleukodystrophy, ALD) 是一種性聯隱性遺傳疾病,導因於 X 染色體長臂 Xq28 位置的 ALDP 基因異常。患者若在無症狀時就先服用「羅倫佐的油」 (Lorenzo's oil),可以降低患者體內非常長鏈飽和性脂肪酸(very long-chain fatty acids; VLCFA) 的含量,減少 VLCFA 異常堆積在大腦白質和腎上腺皮質,進而減緩神經系統的髓鞘 (myelin) 受損。然而,「羅倫佐的油」只能減緩病程、無法「治療」,且對於已有症狀者,效果並不那麼好。
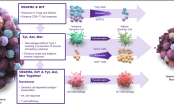
為徹底治療該遺傳疾病,藍鳥生物 (bluebird bio) 使用了反轉錄病毒科中的「慢病毒」(Lentivirus) 作為載體,開發出「eli-cel 基因療法」。8 月 9 日,藍鳥生物宣布,由於在臨床試驗中發現該療法可能導致一名患者在治療一年後,罹患骨髓增生異常綜合症 (一種可能進一步發展為白血病的疾病),且另還有兩名病患骨髓細胞也出現異常、可能發展為骨髓增生異常綜合症,FDA 為此暫停了該試驗。
而就在今年 2 月,在另外的臨床試驗中,使用藍鳥生物另一種基因療法 LentiGlobin 的兩名患者也疑似罹患白血病和骨髓增生異常綜合症,當時藍鳥生物為此暫停了對 β-地中海型貧血和鐮刀型血球貧血的試驗;後來,公司確認其中一個病例是偽陽性,另一例的病症則不是由慢病毒載體所引起 (可能是由為進行治療所做的化療所引起)。然而,這次在 ALD 患者的基因治療上,可就不是這麼回事兒了。
在先前的地中海型貧血和鐮刀型血球貧血患者中所使用的慢病毒載體,其所攜帶的啟動子 (promoter) 只會在紅血球中作用、影響所及只有紅血球;但在 ALD 患者中所使用的慢病毒載體的啟動子,則是種可在所有細胞中作用的強勢啟動子,藍鳥公司的科學家發現慢病毒已經整合到病人的細胞中、破壞了基因調控,顯示該病毒載體推動了類似癌症病症的發展。藍鳥公司首席戰略官 (CSO) 菲爾-葛列格里指出,該療法仍然使大多數患者活著,並且沒有出現與 ALD 相關的主要殘疾,因此認定該療法對患者仍然是有益的。
但是,藍鳥公司所開發的基因療法,面臨的不僅只是安全性問題 (或疑慮) 的挑戰,還有定價問題。早在兩年前,藍鳥生物針對地中海型貧血的基因療法 Zynteglo 在歐洲獲得批准後,便開始談判定價,公司的預期是,在有療效的前題下,定價 180 萬美元/次,可分五年支付;然而,德國政府提出,在 2020 年 11 月到 2022 年 9 月之間,採用 79萬美元/次的臨時價格,若在這之間所有接受治療的患者都感受到療效,德國政府將會補償性地把價格提升至大約 95 萬美元/次。不到一半的價格,讓藍鳥生物決定撤出德國市場,並轉向與義大利、希臘、英國和法國就價格和病患覆蓋率等方面進行討論。評論者認為,藍鳥生物不願意在歐洲降價,是因為他們擔心在美國也必須降價。
但同樣是進行基因療法,諾華 (Novartis) 降低了他們的 Zolgensma (治療脊髓型肌肉萎縮症,SMA) 與 Luxturna (治療一種罕見遺傳視力衰退疾病) 兩款基因療法在歐洲的價格。關於這種「一次治療、終身有效」的療法,諾華的 CEO 直言,「很多醫療系統都沒有準備好去接受可以透過一次治療就提供終生益處的療法」,並認為「首先,國家需要開發新的模型去評估這些新療法能帶來的巨大的好處;其次,大家需要開發出一種新的付款模式,特別是當這個治療的價值是隨著一生而累積的。」一語道破了政府與藥商之間對定價與付款模式產生歧見的主因。
延伸閲讀:《FDA》和歐盟EMA暫停臨床試驗! bluebird bio乙型地中海型貧血的基因療法 Zynteglo 啟動安全調查
資料來源:Endpoints News、Science、CNBC、罕見疾病基金會