《生物相似藥》拜耳與Regeneron眼科重磅藥Eylea專利2027到期!Mylan、Samsung Bioepis、Amgen、Sandoz都來搶食!
Aflibercept為一種血管內皮生長因子(VEGF)抑制劑,可用於治療新生血管性(濕性)老年黃斑部病變(neovasular age-related macular degeneration)、視網膜靜脈阻塞後的黃斑部水腫(macular oedema)、糖尿病黃斑部水腫(diabetic macular oedema)以及糖尿病黃斑部水腫患者的糖尿病視網膜病變(diabetic retinopathy)。
Aflibercept原開發廠產品為拜耳(Bayer)與再生元(Regeneron)共同開發之Eylea (aflibercept),2011年11月成功獲美國食品與藥品管理局(FDA)批准,並於2012年11月獲得歐洲藥品管理局(EMA)的批准。Eylea 於2021年的全球淨銷售額為57.9億美元,使其成為最暢銷的生物製品之一,也是生物相似藥開發商們致力瞄準攻下的一大目標。
台灣bio-CDMO/生物相似藥概念股:泰福(6541)、台康生(6589)、永昕(4726)、中裕(4147)、國光生(4142)、北極星(6550)、保瑞(6472)
Eylea的專利將於2027年6月於美國與歐洲到期,下表為目前已批准或正在開發之Aflibercept生物相似藥或非原開發廠生物製品:
延伸閱讀:學名藥與生物相似藥大舉進攻!2022年即將在美國失去專利保護的10大藥物(Part.1)/學名藥與生物相似藥大舉進攻!2022年即將在美國失去專利保護的10大藥物(Part.2)
延伸閱讀: 《Genet法說筆記》保瑞(6472)回應法說提問:併購伊甸生醫一年挹注營收?與Evofem代工合約挹注多少營收?
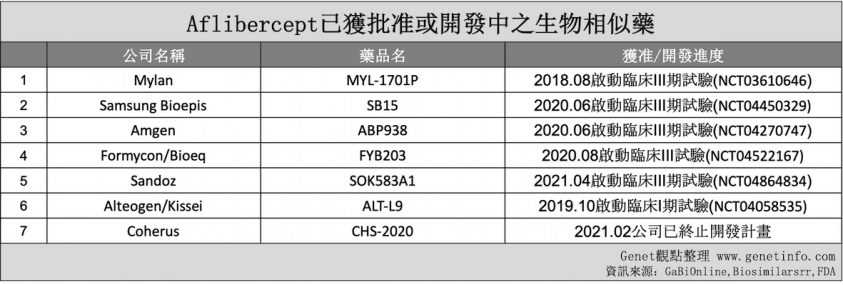
1.Mylan- MYL-1701P(臨床試驗連結)
Mylan與Momenta Pharmaceuticals合作開發之MYL-1701P(也稱為M710),為目前開發進度最快的Aflibercept生物相似藥,於2018年8月啟動臨床III期試驗,共招募324位糖尿病黃斑部水腫(DME)患者以比較MYL-1701P與Eylea的療效與安全性。
2.Samsung Bioepis-SB15(臨床試驗連結)
Samsung Bioepis針對開發中Aflibercept生物相似藥SB15已於2020年6月啟動臨床III期試驗,共招募449位患有新生血管性老年黃斑部病變(nAMD)患者,旨在比較SB15與Eylea之間的療效、安全性、藥物動力學以及免疫原性(immunogenicity)。
3.Amgen-ABP 938(臨床試驗連結)
Amgen旗下開發之Aflibercept生物相似藥ABP 938已於2020年6月啟動臨床III期試驗,共招募579位新生血管性老年黃斑部病變(nAMD)患者,以比較ABP 938與Eylea的療效與安全性,該研究計劃於2022年7月結束。
4.Formycon- FYB203(臨床試驗連結)
由Bioeq GmbH負責管理Formycon旗下開發之Aflibercept生物相似藥FYB203的藥物開發計劃,Bioeq已於2020年8月啟動臨床III期試驗,共招募400位新生血管性老年黃斑部病變(nAMD)患者,以比較FYB203與Eylea的療效與安全性。
5.Sandoz-SOK583A1(臨床試驗連結)
Sandoz針對開發中Aflibercept生物相似藥SOK583A1已於2021年4月啟動臨床III期試驗Mylight,共招募460位患有新生血管性老年黃斑部病變(nAMD)患者,旨在比較SOK583A1與Eylea之間的療效、安全性以及免疫原性。
6.Alteogen-ALT-L9(臨床試驗連結)
Alteogen於2018年1月完成旗下開發之Aflibercept生物相似藥ALT-L9的臨床前試驗,並於2019年10月正式啟動臨床I期試驗,共招募28位新生血管性老年黃斑部病變(nAMD患者,公司已於2021年8月對外表示已完成臨床I期試驗。
7.Coherus- CHS-2020
Coherus BioSciences為Pegfilgrastim生物相似藥Udenyca 的製造商,其針對 Aflibercept生物相似藥候選藥物CHS-2020尚在臨床前開發階段,然而公司已於2021年2月對外宣布終止CHS-2020的相關臨床試驗計劃。
資料來源:GaBiOnline, Biosimilarsrr, FDA
更多資訊,請參考今日彙整。


.jpg)


